Unterrichtsstunde 6: Wie kann man zeigen, dass CO2 ein Treibhausgas ist
| Autoren: | |
| Publikation: | 27.10.2021 |
| Lernstufe: | 3 |
| Ziele: |
|
| Dauer: | 1 Stunde + 15 Minuten Vorbereitung am Vorabend |
| Material: |
Für die ganze Klasse:
|
| Herkunft: | Sonnentaler, Berlin |
Beschreibung des Experiments
Bei diesem Experiment wird der Temperaturverlauf in zwei großen Marmeladengläsern verglichen, die von einer starken Lampe (500 W) beschienen werden. In dem einen Marmeladenglas befindet sich einfach Luft, in dem zweiten wird die Luft teilweise durch CO2 ersetzt.
Dazu wird das CO2 kurz vor der Messung extern produziert, indem Backpulver in ein kleines, halbvoll mit Wasser gefülltes Marmeladenglas gegeben wird. Das entstandene CO2 wird über einen kleinen Schlauch in das zweite Marmeladenglas geleitet. Die Lampe ist in einem Abstand von ca. 20 cm vor den Gläsern angebracht, so dass beide Gläser gleich stark beschienen werden. Um Letzteres zu gewährleisten, muss vor der eigentlichen Messung unbedingt eine Kontrollmessung erfolgen.

Abb. 1: Aufbau des CO2-Experiments
Ziel des Experiments ist zu zeigen, dass die Temperatur in dem mit CO2 gefüllten Glas schneller ansteigt als in dem mit Luft gefüllten.
Der Modellcharakter des Experiments ist nicht einfach zu durchschauen. Beide Gläser sehen gleich aus; man "sieht" nicht, dass sich in dem einen CO2 befindet (höchstens wenn man nach der Messung das Glas öffnet und ein Streichholz hineinhält – das Streichholz erlischt sofort).
Vorbereitung des Experiments und Kontrollmessung
Das Experiment funktioniert nur dann, wenn es sehr genau durchgeführt wird. Der Lehrer sollte es unbedingt ein paar Tage vorher einmal ausprobiert haben.
In die Deckel der Marmeladengläser müssen Löcher gestanzt werden (mit Hilfe eines Henkellocheisens, einer Lochzange oder eines Metallbohrers). Jeder Deckel sollte ein Loch in der Mitte haben, bei den großen Gläsern zum Einführen der Thermometer, bei dem kleinen Glas zum Einführen des Schlauches. Da in das eine Marmeladenglas das CO2 geleitet wird, muss neben dem mittigen Loch für das Thermometer etwas seitlich noch ein weiteres Loch gestanzt werden, um das andere Ende des Schlauches einführen zu können. Nach Einführen von Thermometer oder Schlauch sollte das Loch abgedichtet werden, zum Beispiel mit etwas Knete oder, wie auf dem Foto in Abb. 2, mit einem Durchführungsring aus dem Elektronikhandel.

Abb. 2: Anordnung der gestanzten Löcher in den Deckeln der Marmeladengläser. Ebenfalls sichtbar sind die weißen Papierstreifen vor den Thermometerspitzen.
Inwieweit die Schüler in diese vorbereitenden Arbeiten einbezogen werden, hängt ein bisschen von ihrer Anzahl, ihrem handwerklichen Geschick und der zur Verfügung stehenden Zeit ab. Auch bei der im Folgenden beschriebenen Kontrollmessung, sollte sich der Lehrer überlegen, ob die Zeit reicht, um die Schüler mit einzubeziehen.
Kontrollmessung
Bevor man mit der eigentlichen Messung beginnt, ist es ganz wichtig, dass man eine Kontrollmessung macht. Die beiden Gläser und die Lampe müssen so positioniert werden, dass der Temperaturverlauf in beiden Gläsern gleich ist, wenn sich in beiden "nur" Luft befindet. Es reicht in der Regel nicht aus, die Lampe so aufzustellen, dass sie auf der "Mittellinie" (die genau zwischen beiden Gläsern durchgeht) steht. Dieses exakte Positionieren kann langwierig sein, weil man die Lampe immer wieder ausschalten muss und warten muss, bis die Temperatur wieder gesunken ist. Es ist deshalb eventuell sinnvoll, dass der Lehrer dieses Kalibrieren vorab macht.
Auch wenn die Schüler bei der Kontrollmessung nicht anwesend waren, sollte man ihnen die Wichtigkeit eines solchen Verfahrens vermitteln. Wenn man auf solch eine Kontrollmessung verzichtet, ist das Messergebnis beliebig: Es kann das herauskommen, was man "erwartet", aber genauso gut das Gegenteil.
Worauf man achten sollte
- Die Lampe sollte ziemlich dicht an den Gläsern stehen (ca. 20 cm), damit möglichst viel Wärme in die Gläser gelangt und der im Experiment gemessene Temperaturunterschied möglichst groß ist.
- Um für einen gleichmäßigen Hintergrund zu sorgen, sollte man hinter beide Gläser ein Stück Tonkarton oder Pappe stellen (oder einfach ein Blatt Papier anbringen). Auch hier ist wieder das Ziel, dass die Bedingungen in beiden Gläsern möglichst identisch sind.
- Zum Herstellen des CO2s gibt man nach und nach insgesamt etwa drei bis vier Esslöffel Backpulver in das zur Hälfte mit Wasser gefüllte kleine Marmeladenglas. Der erste Teil des entstehenden CO2s löst sich im Wasser, doch anschließend gelangt das gasförmige CO2 über den Schlauch in das große Marmeladenglas. Man sollte nicht zu viel Backpulver auf einmal in das Wasser geben, damit die aufschäumende Flüssigkeit nicht in den Schlauch (und vor allen Dingen nicht in das große Glas) gelangt.
- Bevor man mit der eigentlichen Messung beginnt, d. h. bevor die Lampe angeschaltet wird, sollte man warten, bis die Temperatur in dem Glas mit CO2 wieder die Temperatur im anderen Glas (also Raumtemperatur) erreicht hat. Durch die Zugabe des Backpulvers steigt die Temperatur im "CO2-Glas" nämlich zunächst leicht an.
- Die Spitzen der Thermometer sollten auf der der Lampe zugewandten Seite durch ein Stück weißes Papier oder Ähnliches "abgeschirmt" sein, da die Thermometerflüssigkeit im Reservoir Wärmestrahlung der Lampe absorbiert. Die Papierabschirmung soll sicherstellen, dass die dadurch verursachte Temperaturerhöhung möglichst klein gehalten wird.
Beispiel einer Messung
Die Schüler sollten 10 Minuten lang jede Minute (besser ist jede halbe Minute) die Temperatur in beiden Gläsern ablesen. Die Messwerte werden in eine Tabelle eingetragen und anschließend in einem Diagramm dargestellt. Das Diagramm in Abb. 3 zeigt ein Beispiel einer Kontrollmessung und Abb. 4 die nach der Kontrollmessung durchgeführte eigentliche Messung, bei der in das zweite Glas CO2 eingeleitet wurde. Man sieht einen zwar kleinen aber deutlichen Unterschied zwischen beiden Kurven: Im Glas mit CO2 ist es nach 10 Minuten um ca. 2,5 Grad wärmer.
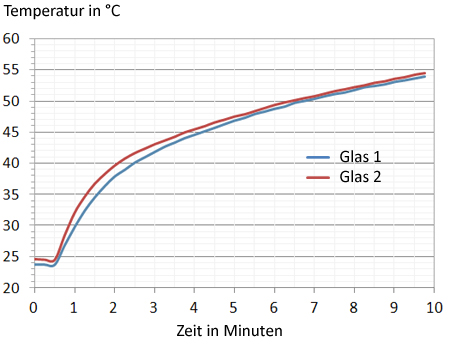
Abb. 3: Kontrollmessung: In beiden Gläsern befindet sich Luft. In das Glas mit dem blauen Temperaturverlauf wird später CO2 eingeleitet.
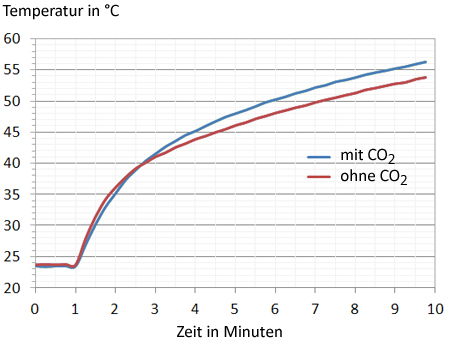
Abb. 4: Eigentliche Messung: In dem einen Glas befindet sich "nur" Luft (rote Kurve), in das andere wurde CO2 eingeleitet (blaue Kurve).
Die Temperaturverläufe der Abbildungen 3 und 4 wurden mit Hilfe von zwei digitalen Thermometern aufgenommen, die an ein CASSY, ein Gerät zur automatischen Messwerterfassung, angeschlossen waren. Das ist natürlich eine sehr bequeme und genaue Messmethode, aber mit einem parallaxefreien Ablesen der Temperatur an zwei normalen Thermometern kommt man zu ähnlichen Ergebnissen.
Schlussfolgerung
Die Schüler stellen fest: Die mit CO2 angereicherte Luft erwärmt sich stärker als die CO2-"arme". Nun kann die Analogie zur Atmosphäre hergestellt werden: Je mehr CO2 die Atmosphäre enthält, desto mehr erwärmt sie sich. Kohlenstoffdioxid ist also ein Treibhausgas.
Diese Schlussfolgerung wird ins Versuchsheft eingetragen zusammen mit einer schematischen Zeichnung.
Letzte Aktualisierung: 29.11.2023






